Tím pod vedením doc. Erika Sedláka odhalil chybu v metodike identifikácií nových liečiv
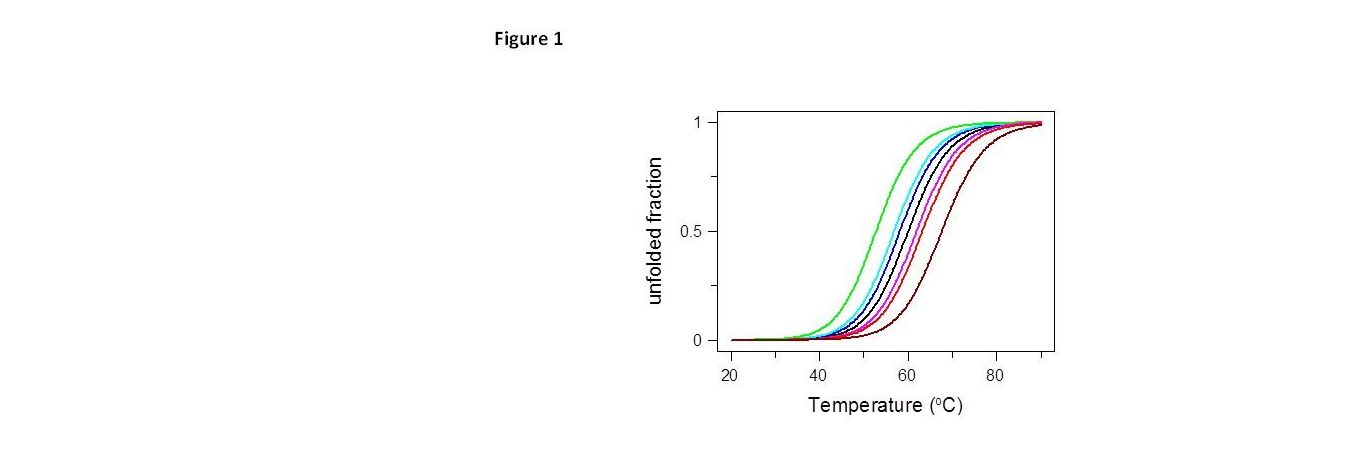
Počiatočné fázy výskumu a hľadania nových liečiv zahŕňajú testovanie obrovského množstva, niekedy až desiatok tisíc, potenciálnych liečiv využitím tzv. vysoko kapacitných biofyzikálnych metód. Potenciálne liečivá, ktoré sa viažu na cieľové molekuly, sú identifikované aj na základe zvýšenej stability cieľových, biologicky významných biomakromolekúl. Pri experimentálnom meraní a analýze stability sa využívajú rozličné biofyzikálne metodiky – napr. pomer intenzít fluorescencie biomakromolekúl pri dvoch odlišných vlnových dĺžkach. Tím pod vedením doc. Erika Sedláka (Centrum interdisciplinárnych biovied – CIB PF UPJŠ) ukázal, že takáto metodika má len veľmi obmedzenú platnosť a môže ohroziť identifikáciu nových liečiv.
doc. RNDr. Erik Sedlák, PhD.: „Naša podrobná analýza ukázala, že pomer fluorescenčných intenzít nie je spoľahlivým parametrom pre určenie stability proteínov a v istých situáciách môže viest k falošne negatívnym záverom, pri ktorom aktívna zlúčenina a potenciálne liečivo je interpretované ako neaktívna látka. V takomto prípade život zachraňujúce liečivo by nebolo zahrnuté do ďalších fáz preklinickeho výskumu. Aby sme predišli takému scenáru, ukázali sme ako zdokonaliť používanú metodiku a navrhli sme možnosti matematickej korekcie. Takmer okamžite sme zaznamenali veľmi pozitívny ohlas zahraničnej farmaceutickej komunity na naše zistenia.“
Na výskume sa podieľal doc. Mgr. Daniel Jancura, PhD. z Katedry biofyziky a CIB PF UPJŠ a bývalý absolvent PF UPJŠ a v súčasnosti vedecký pracovník na Technickej Univerzite v Mníchove (Nemecko), Dr. Gabriel Žoldák.
Kontakt
E-mail: erik.sedlak@upjs.sk
Publikácia
http://onlinelibrary.wiley.com/…227D1.f02t01
Abstract
Monitoring the fluorescence of proteins, particularly the fluorescence of intrinsic tryptophan residues, is a popular method often used in the analysis of unfolding transitions (induced by temperature, chemical denaturant, and pH) in proteins. The tryptophan fluorescence provides several suitable parameters, such as steady-state fluorescence intensity, apparent quantum yield, mean fluorescence lifetime, position of emission maximum that are often utilized for the observation of the conformational/unfolding transitions of proteins. In addition, the fluorescence intensities ratio at different wavelengths (usually at 330 nm and 350 nm) is becoming an increasingly popular parameter for the evaluation of thermal transitions. We show that, under certain conditions, the use of this parameter for the analysis of unfolding transitions leads to the incorrect determination of thermodynamic parameters characterizing unfolding transitions in proteins (e.g., melting temperature) and, hence, can compromise the hit identification during high-throughput drug screening campaigns.